全球疾病负担研究(global burden of disease study, GBD; http: ghdx,healthdata.org/)数据显示脑卒中是我国成人致死、致残的首位病因。中国是最大的发展中国家,人口约占世界总人口的五分之一,卒中患者人数高居世界首位。颈动脉粥样硬化的进展已被证实与脑卒中、短暂性脑缺血发作等脑血管缺血性事件的发生密切相关。近期研究表明,近四分之一的中国成年人存在颈动脉内中膜厚度增加或颈动脉斑块,40-54岁健康人群约1/3可见血管粥样硬化性改变。对个人、家庭和国家健康卫生体系造成巨大负担。因此进一步研究颈动脉粥样硬化的发病机制,寻找新的分子诊疗靶点就具有更加重要的现实意义和理论价值。近日,山东大学齐鲁医院神经外科王东海教授团队在生物医学1区杂志《Theranostics》(IF: 12.4)上发表论文,首次证实了PIM1诱导内皮间质转化(Endothelial to mesenchymal transition, EndMT)促进颈动脉粥样硬化斑块进展的新机制。

颈动脉粥样硬化斑块的发生发展是多种细胞共同相互作用的结果。而内皮细胞损伤和功能失调则是动脉粥样硬化斑块发生的始动环节,内皮损伤刺激因素可导致颈动脉、主动脉和冠状动脉内皮细胞向平滑肌样间充质细胞转化(α-SMA、Snail、Slug表达增高),即EndMT。发生EndMT的内皮细胞丧失内皮特性(VE-cadherin、CD31表达减少),失去内皮细胞的屏障作用,并伴随内皮细胞炎症反应和功能受损。EndMT会使得内皮细胞迁移能力增强并释放促炎趋化因子,导致斑块内新生血管和巨噬细胞浸润,进而加速动脉粥样硬化斑块不稳定破裂。
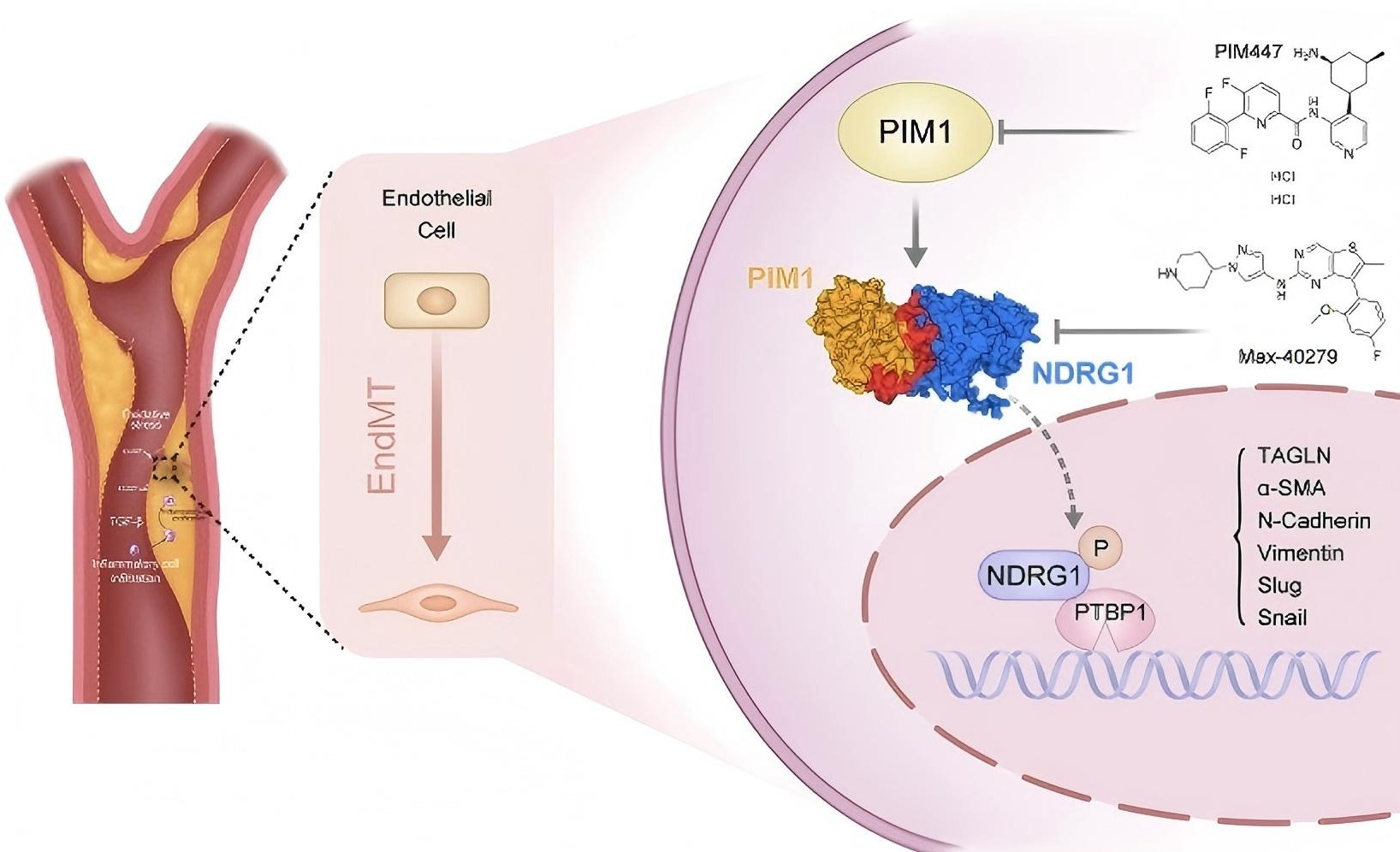
在本研究中,研究人员通过对斑块单细胞测序数据的分析,鉴定出PIM1在晚期动脉粥样硬化斑块的内皮细胞中和发生EndMT的内皮细胞中高表达,抑制PIM1的表达可以显著抑制EndMT。分子机制方面,研究还发现,PIM1可以促进NDRG1在Ser330位点的磷酸化,NDRG1磷酸化后入核增加,进入细胞核后可以与PTBP1结合协作发挥RNA结合蛋白的作用,诱导内皮间质转化,进而促进动脉粥样硬化的进展。随后,研究团队通过分子对接筛选的方式挖掘了可以抑制NDRG1磷酸化并促进NDRG1降解的小分子药物Max-40279,其能有效抑制EndMT,有望成为治疗动脉粥样硬化的新的候选药物。
山东大学齐鲁医院神经外科王东海教授、黄斌副研究员、李新钢教授为文章的共同通讯作者,齐鲁医院神经外科博士研究生薛志伟、韩孟桃,及博士后孙滔为文章的共同第一作者。
该研究获得了山东省自然科学基金项目(编号:ZR2023MH023, ZR2019ZD33)、泰山学者专项基金(tshw201502056)、济南微生态生物医学省实验室基金项目(SYS202202)、齐鲁医院临床实用新技术发展基金(grant 2019-7)以及横向基金(项目编号:11691806 和 6010120062)的支持。
原文链接:https://www.thno.org/v15p0745.htm